G9-1 分子モデリング及びシミュレーションを活用したインシリコ創薬支援
タンパク質構造に基づくインシリコスクリーニング、リガンド設計に向けた分子動力学シミュレーション、タンパク質構造モデリング
[1] 支援担当者
| 所属 | ①筑波大学 医学医療系生命医科学域 | |
|---|---|---|
| 氏名 | ①広川 貴次 | |
| AMED 事業 |
ユニット/領域名 課題名 |
インシリコユニット 分子モデリングおよびシミュレーションを活用したインシリコ創薬支援 |
| 代表機関 代表者 |
筑波大学 広川 貴次 |
|
| 支援技術のキーワード | インシリコスクリーニング、MDシミュレーション、ドッキングシミュレーション、タンパク質立体構造予測 | |
[2] 支援技術の概要
複合要素技術を必要とするインシリコ創薬支援
- ポスト(プレ)ドッキングを必要とするような、難易度の高いドッキング計算、複合体構造モデリング
- Gタンパク質共役型受容体他、創薬標的タンパク質に特化した分子モデリング
- 分子シミュレーションとケモインフォマティクスを融合したタンパク質-リガンド相互作用解析
- タンパク質の動的性質を考慮したインシリコスクリーニング
- 様々な分子モデリング、シミュレーションの要素技術を統合した高度なインシリコ創薬
[3] 支援技術の利用例
- 活性天然物、ペプチドとタンパク質の複合体予測及び相互作用解析による作用機序の理解
- タンパク質の動的性質を考慮した活性部位予測及びヒット化合物からのリード化合物分子設計指針の提供
- Gタンパク質共役受容体のホモロジーモデリング、活性部位予測、リガンド結合予測及び作用機序予測
- 活性ペプチドの低分子化設計
- タンパク質?RNA複合体予測とアプタマー創薬支援
- タンパク質の動的性質を考慮した、構造活性相関解析
[4] 支援担当者の研究概要
近年、構造生物学データを起点とした創薬支援研究が注目されているが、構造生物学データの中には、特定の条件や環境に依存した構造情報であるために、そのままでは創薬へ適用が難しいものがある。分子モデリングや分子シミュレーションは、このような問題を補完できる技術であり、構造生物データと融合させることで、より高度な創薬支援研究が実現可能となる。そのためには、創薬標的タンパク質を中心に、ホモロジーモデリング、ドッキング計算(タンパク質-タンパク質、タンパク質-低分子、タンパク質-核酸、核酸-低分子)、分子動力学計算等の要素技術に基づいた分子モデリング及びシミュレーションを統合的に活用した実用性の高いインシリコ創薬の支援研究と高度化研究が必要だと考えている。
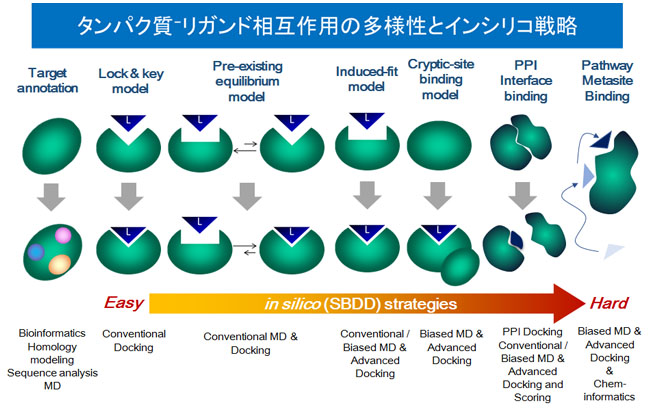
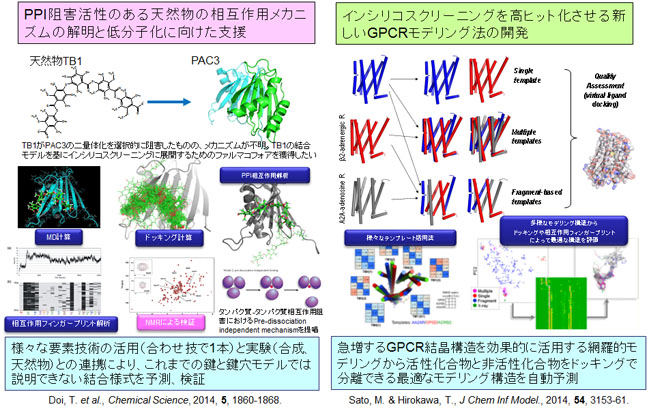
我々は、インシリコスクリーニングに特化したGPCRモデリングツール(Sato M. and Hirokawa T, J. Chem. Inf. Model., 2014)や要素技術を統合化する戦略で、創薬標的となるタンパク質-タンパク質、タンパク質-低分子、タンパク質-核酸、核酸-低分子の分子モデリングに取り組んでいる。代表的な成果として、2014年に発表した、タンパク質-タンパク質相互作用阻害天然物の作用メカニズムを分子モデリング、合成、NMR測定の連携により解明した成果が挙げられる(Doi T et al., Chemical Science, 2014)。この研究課題では、これまでの鍵と鍵穴モデルでは説明できない天然物特有の結合様式を様々な要素技術を活用することで予測が可能となり、実験(合成、天然物)との連携により、予測モデルが正しいことが検証された。
また、2015年の実験情報と統合化インシリコ戦略による活性化Parkin構造の予測(Yamano K, J. Biol. Chem., 2015)では、後に結晶構造にきわめて類似した予測構造を提案したことが明らかになり、本成果は、2015年、JBC Best paper of the weekに選定され、国際的な関心の高さが示された。
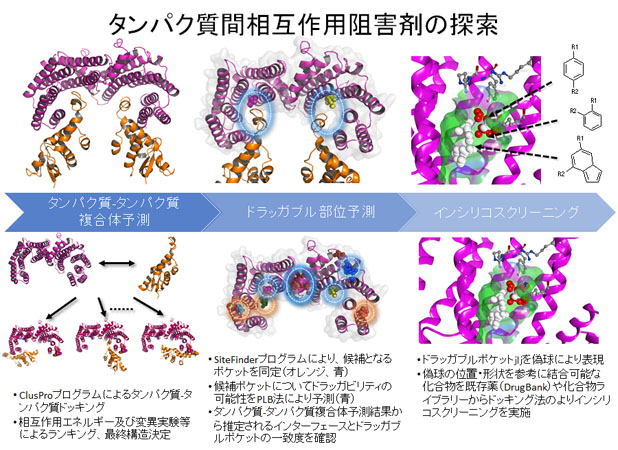
最近の成果として、筑波大学医学医療系の野口雅之研究室との共同研究において初期肺腺癌における標的タンパク質間相互作用阻害薬探索において活性化合物の同定に成功した(Shiba-Ishii A et al., Clin Cancer Res, 2019)。実施内容としては、標的タンパク質であるSFNとSKP1それぞれの立体構造から、タンパク質?タンパク質ドッキング計算でSFN-SKP1複合体を予測した。次に、SFNタンパク質内のSKP1結合部位周辺に存在するポケットのドラッガビリティをコンピュータで評価し、低分子結合が可能であると判断した。この結果に基づき、SKP1と競合する医薬品候補となりうる小分子化合物を、既存薬データベースDrugBankからインシリコスクリーニングし、候補化合物の同定を行った。候補化合物は、共同研究先の筑波大学で様々な生化学実験で評価が行われ、その結果、2つの既存薬において特に強い阻害活性を持ち、さらにヌードマウスを用いた腫瘍抑制効果を有することが確認できた。現在、ドラッグリポジショニングとしての可能性を検討している。様々な構造データベースとインシリコ技術を統合的に活用した創薬支援の成果といえる。